Labtest lança teste rápido para COVID-19
26 mar 2020
A Labtest lança em seu portfólio de testes rápidos um produto específico para auxílio ao diagnóstico do novo coronavírus, SARS-CoV-2, que causa a doença denominada pela OMS de COVID-19.1
O sistema emprega metodologia imunocromatográfica e é utilizado para a detecção qualitativa, rápida, de anticorpos específicos IgG e IgM contra COVID-19 em amostras de soro, plasma e sangue total.
O princípio do teste consiste em anticorpos anti-IgG e anti-IgM humano imobilizados na membrana de nitrocelulose, nas regiões teste IgG e IgM, respectivamente. O conjugado contém partículas de ouro coloidal ligadas aos antígenos recombinantes do COVID-19. Durante o teste, os anticorpos específicos anti-COVID-19 presentes na amostra interagem com o conjugado e migram cromatograficamente através da membrana. Quando encontram as regiões teste, são imobilizados e formam uma linha colorida. A presença desta linha indica um resultado positivo e a sua ausência indica um resultado negativo. Independente do resultado, o ensaio é considerado válido desde que a linha controle apareça.
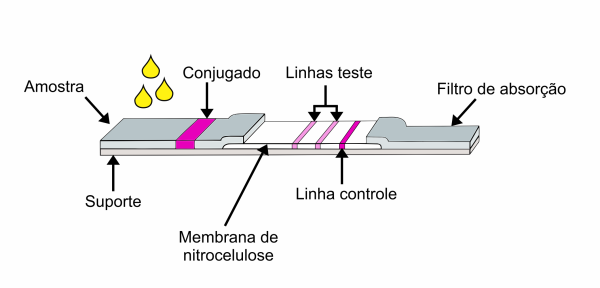
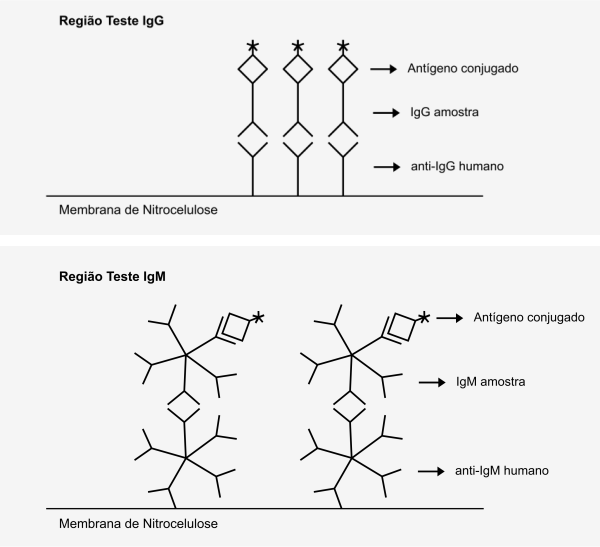
Figura 2. Esquema representativo do princípio do teste
O procedimento é simples, rápido, de fácil interpretação e utiliza-se pequena quantidade de amostra, conforme esta demonstração:
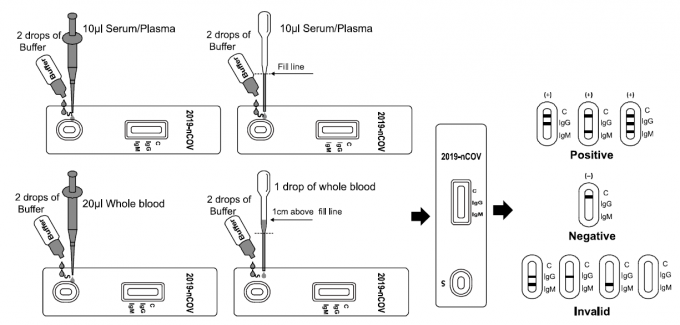
Figura 3. Procedimento e interpretação do teste Anti COVID-19 IgG/IgM Rapid Test
O comparativo foi realizado com 70 amostras, sendo 20 positivas e 50 negativas, determinadas previamente através da técnica de PCR (reação em cadeia da polimerase). O teste apresenta sensibilidade de 85,0% para IgM e >99,9% para IgG e especificidade de 96,0% para IgM e 98,0% para IgG.
A reatividade cruzada foi estudada com amostras positivas para: anti-vírus da influenza A, anti-vírus da influenza-B, anti-RSV, anti-Adenovírus, HBsAg, anti-Sífilis, anti-H. pylori, anti-HIV e anti-HCV. Nenhum resultado falsamente positivo foi encontrado.
A transmissão do novo coronavírus (SARS-CoV-2) entre seres humanos ocorre através do contato com secreções contaminadas do trato respiratório e o período de incubação do vírus é de aproximadamente 3-14 dias.3 Quando uma pessoa é infectada há primeiro a replicação do vírus, que é caracterizada pela alta carga viral (período de viremia) e, em seguida, ocorre a resposta imunológica. O anticorpo IgM é detectado na fase aguda da doença. Com o avanço da infecção, na fase crônica ou convalescente, identifica-se o anticorpo IgG, como mostrado na Figura 4. Na reinfecção, a resposta imunológica é mais rápida e o anticorpo predominante é o IgG.
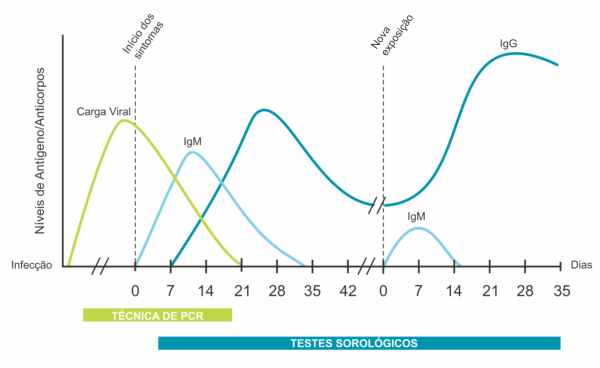
O produto Anti COVID-19 IgG/IgM Rapid Test Ref. 732 possui as seguintes apresentações comerciais: 5, 10, 20, 40 e 100 determinações. De uso profissional, somente para diagnóstico in vitro.
Conte com a excelência técnico-científica da Labtest
Além de oferecer soluções de qualidade e confiança, os produtos com a marca Labtest têm o compromisso maior com a VIDA. A reconhecida excelência da Assessoria Técnico-Científica da Labtest oferece todo o suporte necessário para o acompanhamento do desempenho dos reagentes e suas aplicações, seja no DDG 0800 031 3411 ou no sac@labtest.combr
Para novas informações, entre em contato no Fale Conosco e não deixe de assinar a nossa newsletter.
Referências
- CDC. Centers for Disease Control and Prevention. Human coronavirus types.
https://www.cdc.gov/coronavirus/types.html. Acessado em 17/03/2020. - Willen L, Mertens P, Volf P (2018) Evaluation of the rSP03B sero-strip, a newly
proposed rapid test for canine exposure to Phlebotomus perniciosus, vector of
Leishmania infantum. PLoS Negl Trop Dis 12(8): e0006607.
https://doi.org/10.1371/journal.pntd.0006607 - Kannan S., Shaik Syed Ali P., Sheeza A., Hemalatha K. COVID-19 (Novel
Coronavirus 2019) – recent trends. Eur Rev Med Pharmacol Sci. 2020 Feb; 24(4):2006-
2011. - Turgeon M.L. Immunology & Serology in Laboratory Medicine. Elsevier. 2014, 5
edição
